Die allermeisten Menschen dürften bis Anfang des Jahres 2020 wohl noch nie etwas von Coronaviren gehört haben. Für Experten sind diese Viren, die ihren Namen ihrem kronenartigen Aussehen verdanken, jedoch »alte Bekannte«. Allerdings galten sie bis vor wenigen Jahren als eher harmlose Vertreter, die bei Menschen allenfalls leichte Erkältungssymptome verursachen. Doch das hat sich geändert: Nach SARS und MERS ist SARS-CoV-2 inzwischen das dritte »neuartige Coronavirus«, das eine für Menschen lebensbedrohende Krankheit auslösen kann.
Zu den Personen, die sich schon seit längerem mit — altbekannten wie neuartigen — Coronaviren befassen, gehören die Bioinformatikerinnen und Bioinformatiker um Prof. Dr. Manja Marz von der Universität Jena. Manja Marz leitet das European Virus Bioinformatics CenterExterner Link (EVBC), das an der Jenaer Universität seit 2017 angesiedelt ist. Diesem Zentrum gehören mittlerweile 166 Forscherinnen und Forscher aus 28 Ländern an, darunter sowohl Virologen wie Prof. Dr. Christian Drosten von der Berliner Charité als auch Bioinformatiker.
Werkzeuge für die Corona-Forschung
»Wie die aktuelle Situation sehr eindrücklich zeigt, sind Viren eine ernstzunehmende Gefahr für die menschliche Gesundheit. Das trifft nicht nur für noch zu entdeckende Viren zu, wie jetzt SARS-CoV-2, sondern auch für lange bekannte Viren, die immer wieder neu in unterschiedlichen Weltregionen auftreten«, macht Prof. Marz deutlich. Forschung sei deshalb wichtig. »Obwohl selbst noch in den Kinderschuhen, ermöglicht es die Bioinformatik mit ihren Instrumenten zur Handhabung großer Datenmengen etwa aus Hochdurchsatz-Sequenzierverfahren, viele grundlegende Fragen in der Virologie anzugehen«, so Marz.
Aktuell stehen die Arbeiten am EVBC natürlich ganz im Zeichen von SARS-CoV-2. »Die wissenschaftliche Community hat unheimlich schnell auf das Auftreten des neuartigen Virus reagiert«, sagt Dr. Franziska Hufsky, die wissenschaftliche Koordinatorin des EVBC. Das sei auch wichtig, denn ohne ein möglichst umfassendes Verständnis der Evolution und Pathogenese des Virus ist es vermutlich nicht unter Kontrolle zu bringen. Deshalb werden im EVBC Informationen und bioinformatische Werkzeuge gesammelt, um sie der weltweiten Forschungsgemeinde zur Verfügung zu stellen. Auf seiner Webseite listet das EVBC sämtliche bislang bekannten Tools auf, die speziell auf die Erforschung von SARS-CoV-2 ausgelegtExterner Link sind. Das Spektrum reicht vom einfachen Virennachweis und der Sequenzierung von Virengenomen über die Verbreitung und Evolution bestimmter Viruslinien bis hin zu Werkzeugen, die geeigneten Angriffspunkte für Medikamente ausfindig machen.
Bioinformatikerin Franziska Hufsky ist wissenschaftliche Koordinatorin des Europäischen Virus-Bioinformatik-Zentrums der Universität Jena. In einer Übersichtsarbeit hat sie die wichtigsten Werkzeuge aus der Bioinformatik zur Erforschung von SARS-C-V-2 zusammengefasst.
Foto: Anne Günther (Universität Jena)Das eine Coronavirus löst Schnupfen aus — das andere COVID-19
In einer aktuellen ÜbersichtsarbeitExterner Link haben Franziska Hufsky, Manja Marz und ihr Jenaer Team jetzt die wichtigsten Werkzeuge zusammengefasst, die über 50 Forscherinnen und Forscher aus aller Welt für jedermann kostenfrei zur Verfügung gestellt haben. Natürlich ist auch diese Publikation online frei zugänglich auf der Seite des EVBC zu finden. »Die Corona-Krise zeigt gerade sehr schön, wie Wissenschaft im besten Falle funktioniert: international, fachübergreifend, kooperativ«, sagt Franziska Hufsky. Einrichtungen wie das EVBC spielen dabei eine wichtige Rolle, unterstreicht die Bioinformatikerin. »Sie dienen als Treffpunkt zum wissenschaftlichen Austausch, als Ideenschmiede und Werkstatt, und bringen die Forschung einfach schneller voran.«
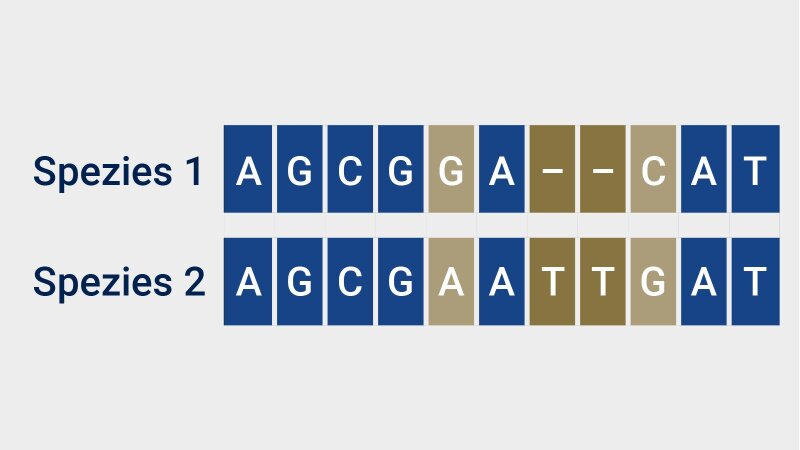
Hufsky und ihre Kollegen engagieren sich jedoch nicht nur als Wissenschaftskoordinatoren über das EVBC. Die Jenaer Bioinformatiker betreiben auch selbst Viren-Forschung und stellen ihre Ergebnisse der Community zur Verfügung, so wie Kevin Lamkiewicz. Der Doktorand erstellt und untersucht sogenannte virale Alignments. »Dabei handelt es sich um die Gegenüberstellung von Genomsequenzen unterschiedlicher Spezies, wobei identische oder sehr ähnliche Sequenzabschnitte übereinander angeordnet werden«, erläutert Lamkiewicz. Durch ein solches Arrangement lassen sich Gemeinsamkeiten und Unterschiede im Erbgut leichter erfassen und vor allem diejenigen Sequenzbereiche identifizieren, die sich auf Eigenschaften der kodierten Eiweiße auswirken könnten.
Derzeit studieren die Bioinformatiker zum Beispiel Alignments des neuartigen Coronavirus SARS-CoV-2 mit dem Human Coronavirus 229E (HCoV-229E), einem seit Jahrzehnten bekannten Erkältungsvirus. »Uns interessiert, wie es sein kann, dass HCoV-229E lediglich eine harmlose Erkältung auslöst, während SARS-CoV-2 binnen weniger Wochen die ganze Welt stilllegt.«
Bioinformatik-Doktorand Kevin Lamkiewicz untersucht die Sekundärstruktur von Viren-RNA, unter anderem von SARS-CoV-2.
Foto: Anne Günther (Universität Jena)Klar ist, nicht jeder Unterschied in der Genomsequenz wirkt sich auf die Funktionalität der Virus-Eiweiße aus. Oftmals ist es sogar so, dass es während der Virusvermehrung zu Kopierfehlern (Mutationen) kommt, die sich überhaupt nicht bemerkbar machen (»stille Mutationen«). »Andererseits kann aber auch eine einzige Mutation dazu führen, dass sich das Virus nicht mehr vermehren kann«, so Lamkiewicz. Genau das konnte er mit einigen Kollegen in einer Studie für HCoV-229E zeigenExterner Link: die virale Replikation verringert sich drastisch, wenn sich an Position 47 ein Guanin anstelle eines Cytosins befindet. Solche Bereiche wollen die Forscher jetzt für SARS-CoV-2 ausfindig machen, da sie vielversprechende Angriffspunkte für potenzielle Therapien gegen das Virus wären.
Ausschnitte aus Gensequenzen zweier Spezies (z. B. Viren) im sogenannten Alignement. Dabei werden einander entsprechende Sequenzbereiche gegenübergestellt und verglichen. Identische Sequenzbereiche sind blau dargestellt. Die blass-goldenen Bereiche weisen Unterschiede auf, die durch Mutationen entstanden sein können. Der Abschnitt in gold markiert eine Deletion bei Spezies 1.
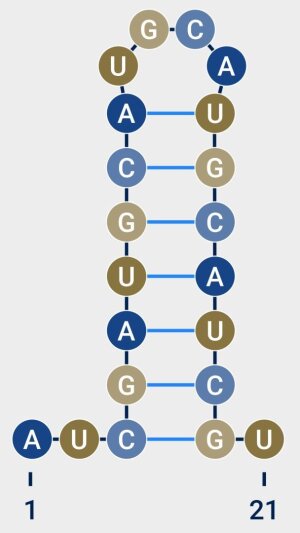
Abbildung: Kevin Lamkiewicz, bearbeitet von Liana FrankeRNA-Sekundärstruktur. Die blauen Linien stehen für Interaktionen von Nukleotidbasen, die nicht benachbart liegen und so zur Ausbildung von räumlichen Strukturen der RNA führen.
Abbildung: Kevin Lamkiewicz, bearbeitet von Liana FrankeDass vergleichsweise geringe Änderungen in den Erbinformationen gewaltige Auswirkungen auf die Eigenschaften des Virus haben können, liegt an der Sekundärstruktur der Genomsequenzen. Diese bestehen im Falle der Coronaviren aus RNA (Ribonukleinsäure), also einsträngigen Ketten aneinandergereihter Nukleotide. Die einzelnen Nukleotide können miteinander interagieren, auch wenn sie nicht direkt benachbart in der Kette liegen. Dadurch entstehen strukturelle Elemente wie haarnadelförmig gepaarte Stränge oder Loops, die essenziell für die Virusvermehrung sein können. »Änderungen in der Nukleotidabfolge können zu Änderungen in der Sekundärstruktur führen, was sich unter Umständen auf ihre Funktionalität auswirkt«, erläutert Kevin Lamkiewicz.
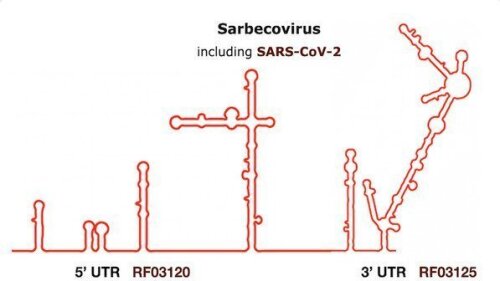
Die Jenaer Bioinformatiker haben aktuell für SARS-CoV-2 und alle bisher bekannten Coronaviren (darunter HCoV-229E) Teil-Alignments für diejenigen Genombereiche erstellt, die für die Ausbildung von RNA-Sekundärstrukturen wichtig sind und in der Datenbank „Rfam“ hinterlegt. Darauf können nun experimentell arbeitende Forschungsteams weltweit zugreifen und schauen, ob sich diese Strukturen als Ansatzpunkte für Therapien nutzen lassen.
Mini-Seqenziergerät liefert komplettes Virengenom
Damit Genomsequenzen von Viren überhaupt untersucht werden können, müssen diese natürlich erst einmal bekannt sein. Und auch daran arbeiten die Bioinformatiker der Universität Jena. Gemeinsam mit Forscherinnen und Forschern des Uniklinikums sequenzieren sie im Rahmen des nationalen Konsortiums NFDI4MicrobiotaExterner Link seit März regelmäßig die im Uniklinikum anfallenden Proben von COVID-19-Patienten. Dafür nutzen sie das MinION System – ein kleines mobiles Sequenziergerät, das, kaum größer als ein USB-Stick, direkt an einen Laptop oder PC angeschlossen werden kann (Foto oben).
Diese Sequenziertechnik ist im Jenaer Team bereits seit längerem etabliert. Neben seiner geringen Größe und einfachen Handhabung biete das MinION System gegenüber bisherigen Sequenzierungsmethoden weitere praktische Vorteile, erklärt Doktorand Sebastian Krautwurst, der in diesem Projekt arbeitet. »Zum einen lassen sich ganze Genome am Stück sequenzieren, während bisherige Verfahren meist nur Teilsequenzen geliefert haben, die anschließend zusammengefügt werden mussten.« Zum anderen kann mit dem Mini-Sequenzierer RNA direkt analysiert werden — bislang war zuvor eine Übertragung in DNA notwendig.
Doktorand Sebastian Krautwurst sequenziert RNA aus COVID-19-Patientenproben.
Foto: Anne Günther (Universität Jena)Bei der Sequenzierung mit dem MinION Gerät werden DNA- oder RNA-Stränge einzeln durch winzige Tunnel — sogenannte Nanoporen — gezogen. Währenddessen wird der elektrische Stromfluss gemessen und registriert, wie sich dieser verändert, während die einzelnen Nukleinbasen (Adenin, Guanin, Cytosin, Thymin oder Uracil) die Pore passieren. Diese Veränderungen sind spezifisch für jede Base und so lässt sich im Nachhinein ihre exakte Abfolge — also die Sequenz — bestimmen.
Sebastian Krautwurst und seine Teamkollegen haben mit dieser Technik bereits unterschiedliche Stämme von HCoV-229E und das Gastroenteritisvirus (TGEV) sequenziert. Nun widmen sie sich verstärkt der Sequenzierung von SARS-CoV-2-Proben.
Text: Ute Schönfelder